Фенол его вред и польза
Чем опасен фенол
Фенолами называют органические вещества, в состав которых входит одна или несколько гидроксильных групп, присоединенных к углероду бензольного кольца. Простейший фенол, называемый также карболовой кислотой, имеет формулу C6H5OH. Температура плавления фенола невысока – 40,9°С, поэтому при обычных условиях фенол представляет собой бесцветные кристаллы, которые немного полежав на воздухе, приобретают розоватый оттенок.
Фенол – летучее вещество с характерным резким запахом. Пары его ядовиты. При попадании на кожу фенол вызывает болезненные ожоги.
В химической промышленности фенолы используют для изготовления красителей, пестицидов, лекарственных препаратов, фенолформальдегидных смол и синтетических волокон. Прежде фенол в виде разбавленного раствора применялся в качестве антисептика (т.н. «карболка») для дезинфекции белья и помещений. И сегодня в состав многих чистящих и дезинфицирующих растворов тоже входят различные фенолы, которые действуют как бактерицидные средства. Фенолы добавляют в пестициды и фунгициды, также они используются как консерванты для клея и древесины.
Сфера применения этих веществ достаточно широка, но большинство жителей нашей страны узнало о них из-за скандала, разразившегося в конце 1990-х гг. вокруг печально известных «фенольных домов» – панельных многоэтажек серии П-49/П, построенных в конце 1970 – начале 1980-х гг.
Эти дома в свое время считались экспериментальными. В бетон, использованный при их строительстве, добавляли фенолформальдегид. Это должно было ускорить его затвердевание и тем самым приблизить сроки сдачи домов. А для удешевления процесса в качестве утеплителя панелей было решено использовать стекловату, пропитанную фенолформальдегидными смолами. Ею заполнялись межплиточные стыки. Практически сразу после того как «фенольные дома» были построены, по их стенам поползли трещины, герметичность швов нарушилась, и ядовитые фенольные испарения поползли внутрь квартир. Причиной этому стали и ошибки проектировщиков, и несовершенство технологии производства и монтажа сборных конструкций. Но вряд ли эти объяснения смогут как-то успокоить людей, получивших квартиры в таких домах.
Всего в 70-80-е годы в Москве было построено 5,7 млн. кв. метров типового жилья серии II-49/П. Сложно в точности сказать, сколько из них стали объектами «эксперимента». По утверждениям городских властей, в городе сегодня числится около 260 «фенольных домов». Часть из них находится на востоке Москвы – на Открытом шоссе и улице Николая Химушина.
Новоселы, поначалу обрадовавшиеся просторным квартирам, вскоре поняли, что вместе с новым жильем они получили целый букет проблем со здоровьем – это и аллергия, и болезни глаз, почек, дыхательных путей, и даже злокачественные новообразования.
Дело в том, что фенол и его производные без труда проникают в организм человека через кожу и желудочно-кишечный тракт, а пары фенола – через легкие. В организме фенол легко образует соединения с другими веществами, присутствующими в организме. Чем выше концентрация фенола в крови, тем сильнее его неблагоприятное влияние на здоровье человека. Продукты взаимодействия фенола с другими веществами, а также часть несвязанного фенола выводятся с мочой.
О наличии фенола в организме можно узнать по анализу мочи. Он также помогает определить, что данный человек отравился фенолом либо веществами, которые превратились в его организме в фенол. Но один только анализ мочи не позволит утверждать, что больной стал жертвой отравления именно фенолом, так как многие химические вещества, попадая внутрь организма, вступают в химические реакции с образованием этого вещества.
Поэтому, если возникают подозрения, что в питьевой воде либо в воздухе жилого или рабочего помещения присутствует фенол либо его пары, лучше заказать соответствующее лабораторное исследование, ведь отравление фенолами – и острое, и хроническое – представляет реальную угрозу не только здоровью, но и жизни человека.
Симптомы отравления фенолом
При остром отравлении, сопровождающем попадание фенола на кожу или вдыхание его паров, наблюдается сильное жжение в местах, подвергшихся его непосредственному воздействию. Проявляются ожоги слизистых тканей; возникает сильная боль в области рта, в глотке, животе; тошнота, рвота, понос; резкая бледность, слабость, отек легких; возможны острые аллергические проявления; артериальное давление понижено; развивается сердечно-легочная недостаточность, возможны судороги; моча бурая, быстро темнеет на воздухе.
Первая помощь – снять одежду (желательно сразу под душем), промыть пораженное место большим количеством воды. Прикрыть места ожогов фенолом чистой белой тканью. Если брызги фенола попали в глаза, необходимо обильно промывать их водой не менее 15 минут. Промыть желудок водой, внутрь дать активированный уголь. Спирт и вазелиновое масло противопоказаны. Во время стационарного лечения больному даются обволакивающие средства и анальгетики, подается О2 с обеспечением адекватной вентиляции легких, производится коррекция водноэлектролитного баланса.
Хроническое отравление фенолом приводит к анорексии – прогрессирующей потере веса; вызывает диарею, головокружение, трудности при глотании, обильное отделение слюны. При хроническом отравлении фенолами отмечено темное окрашивание мочи. Ученые, исследовавшие последствия фенольных отравлений указывают, что в результате длительного пребывания под воздействием фенола человек может чувствовать боли в мышцах, слабость. Печень у таких людей увеличена. Хроническое отравление фенолом вызывает поражения центральной нервной системы, нервные расстройства, сопровождаемые головными болями и потерей сознания, а также поражения почек, печени, органов дыхания и сердечно-сосудистой системы.
По сообщению Управления по охране окружающей среды США (EPA), максимальная доза фенола, которая условно безопасна при попадании внутрь организма человека, составляет 0,6 мг/1 кг живого веса в течение 1 суток. Данная доза рассчитана без учета возможного канцерогенного эффекта фенолов, который способен проявиться спустя достаточно большой период времени. Следует отметить, что указанная величина служит исключительно в качестве точки отсчета: она показывает, что при концентрациях фенола выше данной, вероятность неблагоприятных последствий для здоровья человека резко возрастает. Аналогичным образом EPA устанавливает допустимое содержание фенола в воздухе – оно составляет 0,006 мг/м3.
В нашей стране ПДК фенола в жилой зоне составляет 0,03 мг/м3 (СанПин 2.1.2.1002-00), а в воздухе рабочей зоны – 0,3 мг/ м3.
Запах фенола – сильный и сладковатый – начинает ощущаться, если концентрация фенола в воздухе превышает 0.04 ppm (0.000004%)
Хроническое отравление фенолом угрожает не только жителям «фенольных домов». Недобросовестные изготовители мебели, строительных и отделочных материалов, лакокрасочных изделий, декоративной косметики и даже детских игрушек могут пренебречь требованиями безопасности и выпускать продукцию с недопустимо высоким содержанием таких токсичных веществ, как фенолы и производные.
Помните, если вас настораживает неприятный запах недавно приобретенной вещи, если вам кажется, что ваше здоровье после покупки мебели или недавнего ремонта пошатнулось, будет лучше вызвать специалиста-эколога, который проведет все нужные исследования и даст необходимые рекомендации, чем пребывать в тревоге и сомнениях, опасаясь за свое здоровье и здоровье своих близких.
Ирина Карпенко,
инженер-эколог ООО «Экосистем»
https://www.ecoekspert.ru
Источник
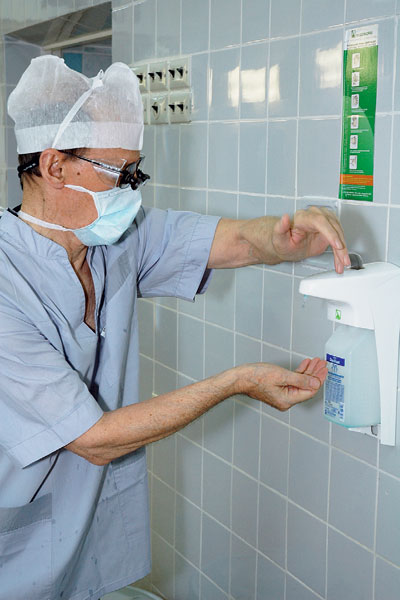
Первым антисептиком в хирургии был раствор фенола (карболовой кислоты). Сейчас хирурги обеззараживают руки более щадящими средст-<br />вами. На фото: академик А.В.Покровский готовится к операции. Фото Дмитрия Зыкова.
‹
›
Ещё в XVI веке знаменитый немецкий врач и естествоиспытатель Парацельс сказал: «Всё есть яд, и ничто не лишено ядовитости, одна лишь доза делает яд незаметным». Это на самом деле так. Даже обычная поваренная соль может стать причиной смерти, если съесть её больше трёх граммов на килограмм веса. И наоборот, ядовитые вещества при определённой дозировке и небольшой химической модификации могут превратиться в очень даже полезные для организма. Одно из таких веществ – фенол, или карболовая кислота (C6H5OH).
Игольчатые кристаллы фенола настолько ядовиты, что при контакте с кожей вызывают её поражения и ожоги, а вдыхание паров фенола приводит к расстройству нервной системы, нарушению работы органов дыхания и сердца. В химических лабораториях с фенолом работают в защитных перчатках и в вытяжном шкафу – это специальное рабочее место, встроенное в шкаф с вытяжной вентиляцией, выводящей опасные пары из помещения. Между тем именно с фенола началась эра антисептиков.
В конце 1860-х годов английский хирург лорд Джозеф Листер (1827-1912) первым применил раствор карболовой кислоты в медицинских целях. С помощью карболки он боролся с нагноениями ран при открытых переломах. Сегодня соединения фенола входят в состав многих медицинских препаратов. Его применяют для дезинфекции животноводческих ферм, различных хранилищ, обеззараживания спецодежды, белья, инструментов и многого другого. Производство фенола достигло 8,3млнтонн в год. Среди всех веществ, производимых мировой химической промышленностью, по объёму выпуска фенол стоит на 33-м месте.
Производные фенола входят в состав парацетамола – лекарства, которое назначают для лечения простуды и гриппа; содержатся они и в листьях вкусной и полезной ягоды брусники. Чтобы убедиться в этом, проведём два несложных химических эксперимента.
Нам потребуется хлорид железа (FeCl3)- его можно купить в магазине радиотехники, а парацетамол в таблетках и сбор листьев брусники приобретём в аптеке.
Начнём с того, что растворим в горячей воде таблетку парацетамола и добавим немного хлористого железа. Почти сразу раствор посинеет, так как в нём образуется сине-фиолетовое комплексное соединение фенола с солями железа.
Реакция образования комплекса фенола с железом:
6C6H5OH+FeCl3→[Fe(C6H5OH)6]Cl3.
Точно такие же изменения мы обнаружим, если проведём эксперимент с настоем из листьев брусники (рис. 1).
Ещё одна реакция, которую можно провести в домашних условиях,- окисление фенола в хиноны, которые имеют интенсивную окраску. Фенол вступает в реакцию очень легко: даже под воздействием воздуха его белые кристаллы окисляются и приобретают розоватый цвет.
Нам понадобятся таблетка парацетамола и обычный отбеливатель, содержащий гипохлорит натрия (NaOCl), который продаётся в хозяйственных магазинах.
Таблетку парацетамола растворим в горячей воде и добавим небольшое количество отбеливателя. Почти сразу раствор окрасится в интенсивный коричневый цвет. Происходит это потому, что входящий в состав отбеливателя гипохлорит натрия окисляет парацетамол в соединение1, которое в растворе постепенно переходит в соединение2 (рис. 2). Оба они относятся к хинонам.
Источник
Историческая справка
Фенол был открыт Фридлибом Фердинандом Рунге в 1834 году при перегонке каменноугольной смолы. Он назвал ее карболовой кислотой или угольной кислотой (карбон = уголь, олеум = масло) из-за ее кислотного действия в водном растворе.
Первое значительное применение фенола принадлежит английскому хирургу Джозефу Листеру (1827-1921). Листера вдохновила микробная теория болезней Луи Пастера (1822-1895) и он начал использовать антисептические методы во время своих операций в 1860-х годах. В своей борьбе с раневыми инфекциями, которые часто возникали после операций, он применил так называемую «карболовую повязку» в 1865 году. Это позволило ему в значительной степени предотвратить серьезные и опасные для жизни нагноения хирургических ран. Листер также разработал основы больничной гигиены. Частое мытье рук врачами и медперсоналом раствором фенола и использование резиновых перчаток дали прекрасные результаты и смертность пациентов резко упала. В истории медицины Листер считается «отцом антисептики».
В молекулярной биологии экстракция органических тканей смесями фенола, хлороформа и изоамилового спирта была одним из первых методов получения ДНК высокой чистоты.
Производство фенола
Есть три важных технических процесса для синтеза фенола:
- В прошлом фенол экстрагировали из дистиллята при перегонке каменноугольной смолы. Фенолят натрия получали добавлением к дистилляту раствора гидроксида натрия, который можно было разложить на фенол добавлением соляной кислоты.
- В промышленных масштабах бензол превращается в изопропилбензол (кумол) реакцией с пропеном. Гидропероксид кумола получают в результате реакции с кислородом. Кислоты расщепляют эту перекись на фенол и ацетон. Экономичность процесса особенно высока, потому что производятся два важных химических материала. Сегодня это наиболее предпочтительный способ производства фенола. Бензол и пропен первоначально превращаются в кумол путем алкилирования. Затем кумол окисляется кислородом с образованием гидропероксида. Последующая кислотная обработка дает фенол и ацетон в реакции перегруппировки. Этот процесс крайне экономичен из-за попутно производимого ацетона.
- Гидролиз хлорбензола гидроксидом натрия при 250 C и давлении в от 2 до 5 МПа дает в результате искомый фенол.
Характеристики и свойства фенола
Фенол (гидроксибензол) – самый простой представитель класса фенолов. Фенол токсичен и редко встречается в природе в чистом виде, и поэтому в основном производится синтетическим путем. Содержится в каменноугольной смоле, которая образуется при дегазации угля (коксовании), в небольших количествах в древесине сосны и хвое.
Фенолы формально являются производными бензола. Его основная структура представляет собой ароматическое бензольное кольцо, в котором один или несколько атомов водорода бензола замещены гидроксильной группой. В воде фенол слабо диссоциирует на протоны и фенолят-анион. Это также объясняет хорошую растворимость фенола в разбавленном щелоке.
Фенол ядовит, образует бесцветные кристаллические иглы, которые на воздухе становятся красноватыми и постепенно растворяются. Молярная масса 94,1 г / моль. Плавится при 43 C, кипит при 182 C и имеет плотность 1,132 (при 25 С). Обладает характерным резким запахом. Очень хорошо растворяется в эфире, хлороформе, эфирных маслах и спирте, умеренно в бензоле и воде и очень трудно в алифатических углеводородах.
Токсичность фенола основана на его повреждающем действии на протоплазму клеток. Из-за этого бактерицидного свойства фенол или растворы, содержащие фенол (макс. 5% фенола), ранее использовались в качестве дезинфицирующих средств в хирургии.
В отличие от спиртов фенол реагирует характерным образом с разбавленным раствором хлорида железа (III). Раствор становится сине-фиолетовым. Эта цветная реакция используется в качестве доказательства присутствия фенола. Фенол можно заставить реагировать со многими другими соединениями, и поэтому он является важным исходным материалом в синтетической органической химии.
В отличие от алифатических спиртов фенолы не подвергаются реакциям нуклеофильного замещения с заменой гидроксильной группы другими нуклеофилами. Из-за электронодонорной природы гидроксигруппы фенол примерно в тысячу раз более активен, чем бензол.
Порог запаха в воздухе составляет 0,04 частей на миллион, а в воде – 7,9 частей на миллион.
Соли фенола
При взаимодействии с щелочными металлами образуются феноляты (соли). Феноляты (в отличие от алкоголятов) достаточно устойчивы в воде. Кроме того, в ароматическом кольце могут протекать реакции с образованием различных производных фенола.
Одним из примеров является образование салициловой кислоты (2-гидроксибензойной кислоты) в результате реакции фенола с диоксидом углерода при интенсивном нагревании. Салициловая кислота является промежуточным продуктом для производства известного лекарственного препарата аспирин (ацетилсалициловая кислота), в котором фенольная гидроксильная группа все еще ацетилирована.
Производные фенола
Важное значение имеют не только сам фенол, но и его производные. Это соединения, которые имеют другие функциональные группы в ароматическом кольце помимо группы ОН, такие как уже упомянутая салициловая кислота.
Эти вещества (например, ванилин) как правило, имеют довольно приятный запах и широко распространены в природе. Их используют в парфюмерной промышленности в качестве ароматизаторов.
- Фенольные смолы – это синтетические смолы, образующиеся в результате конденсации альдегидов (особенно формальдегида) с фенолом. В основном они используются для производства фенопластов.
- Фенолфталеин – это органический краситель, который бесцветен в кислых и нейтральных растворах и становится розовым в щелочных растворах. Фенолфталеин – один из наиболее широко используемых индикаторов для кислотно-основного титрования.
Многоатомные фенолы
- Одновалентный: фенол (гидроксибензол).
- Двухвалентный: пирокатехол (1,2-дигидроксибензол), резорцин (1,3-дигидроксибензол), гидрохинон (1,4-дигидроксибензол).
- Трехвалентный: пирогаллол (1,2,3-тригидроксибензол).
Если атом углерода дополнительно замещен одной или несколькими электроноакцепторными группами, например с нитрогруппой, кислотный характер фенольной группы -ОН значительно усиливается и может почти достигать силы некоторых минеральных кислот (например, HCl, HNO3).
Содержание в продуктах
Фенол содержится в более чем 150 натуральных продуктах, включая, абрикос, вишню, черную смородину, чернику, клюкву, другие ягоды, виноград, фрукты гуавы, персик, ананас, спаржу, лук, вареный картофель, помидоры, кору корицы, лист кассии, имбирь, сыр, масло, молоко, сухое молоко, вареное яйцо, рыба и рыбий жир, колбасы и колбасы, пиво, пшеничный хлеб, хрустящий хлеб, коньяк, розовое вино, какао, кофе, чай, виски, жареный фундук, жареный арахис, соя, орехи пекан, мед, авокадо, арктическая ежевика, маракуйя, бобы, грибы, табак, вареная говядина и курица, ферментированный соевый соус, жареный миндаль, семена кунжута, пажитник, манго, тамаринд, бразильский орех, рис, ревень, солодка, гречка, кресс-салат, креветки, крабы, раки, моллюски, кальмары, трюфель и китайская айва.
Применение
В настоящее время фенол преимущественно используется для изготовления фенольных смол, которые находят самое широкое применение в строительной отрасли. Они используются в качестве связующих веществ и наполнителей в деревянных изделиях, таких как фанера, ДСП, мебель и панели. Феноловые смолы пропитываются бумагой, которая после затвердевания дает листы, которые можно склеивать, чтобы сформировать ламинат для использования в стеновых панелях и столешницах.
Как мощный бактерицид, фенол можно найти во многих потребительских товарах, включая жидкости для полоскания рта, антисептические мази, леденцы для горла, освежители воздуха, ушные капли и бальзамы для губ.
Фенол продолжает оставаться основным химическим веществом, используемым для производства термореактивных смол. Эти смолы производятся путем объединения фенола с альдегидами, такими как формальдегид.
Помимо строительной промышленности, фенол находит множество других применений. Он используется в фармацевтике, в гербицидах, пестицидах и красках. Его можно использовать для производства капролактама, который является мономером, используемым при производстве нейлона. Другим важным промышленным соединением, получаемым из фенола, является бисфенол А, который производится из фенола и ацетона. Бисфенол А используется при производстве поликарбонатных смол, для дпльнейшего использования в различных продуктах, таких как автомобильные детали, электротехнические изделия и потребительские товары: компакт-диски, очки для чтения, солнцезащитные очки и бутылки с водой.
Фенол используется для производства множества органических соединений, таких как пирокатехин, резорцин, анилин, салициловая кислота, пикриновая кислота, адипиновая кислота, пластмасс, фенольных смол, фенолфталеина (индикатор), пикриновой кислоты, фармацевтических препаратов, инсектицидов, консервантов для древесины, взрывчатых веществ, дубильных веществ и многого другого.
Широко используется в качестве дезинфицирующего средства в нефтяной, кожевенной, бумажной, мыльной, игрушечной, кожевенной, красильной и сельскохозяйственной промышленности.
В микроскопии он используется для производства фенольной воды, состоящей из десяти частей фенола и одной части воды.
Опасность для здоровья
Фенол очень токсичен: вероятная летальная доза при пероральном приеме (для человека) составляет 50-500 мг / кг. Проглатывание всего 1 грамма уже является смертельной дозой. Люди, страдающие заболеваниями печени или почек, подвергаются большему риску.
Фенол очень быстро всасывается через поверхность кожи, легких и желудка. Симптомы отравления включают, помимо прочего, рвоту, затруднение глотания, диарею, отсутствие аппетита, головную боль, обмороки, головокружение, психические расстройства и кожную сыпь. Прямой контакт с фенолом вызывает жжение во рту, раздражение глаз, носа и дерматит, изменение цвета кожи и повреждение печени и почек. Известно, что воздействие фенола в различных концентрациях вызывает психические расстройства, угнетение ЦНС и кому.
Фенол раздражает кожу, но обладает местным анестезирующим действием, поэтому при первом контакте с ним боль не ощущается. Обычно происходит побеление области контакта, а позже могут развиться тяжелые ожоги. Фенол быстро всасывается через кожу, и токсичные или даже смертельные количества могут абсорбироваться через относительно небольшие участки. Воздействие паров фенола может вызвать сильное раздражение глаз, носа, горла и дыхательных путей.
Острое воздействие может привести к тошноте, рвоте, мышечной слабости и коме. Попадание фенола в глаза может вызвать серьезные повреждения и, возможно, слепоту.
Исследования на животных показали, что фенол может быть репродуктивным токсином.
Абсорбция фенола через неповрежденную кожу, как определено по уровням фенола в крови у подопытных животных, зависела от поверхности нанесения, а не от его концентрации в исследуемых растворах. Животные (свиньи) проявляли признаки подергивания и тремора в течение нескольких минут после нанесения, за которыми следовало слюноотделение, выделения из носа и затрудненное дыхание.
Пожароопасность
Фенол – твердое горючее вещество. При нагревании фенол выделяет пары, которые являются взрывоопасными при концентрации от 3 до 10% в воздухе. Для тушения фенольных пожаров следует использовать углекислотные или сухие химические огнетушители, т.к. сток воды для пожаротушения может выделять ядовитые газы и вызывать загрязнение.
Источник
